详解2019诺贝尔化学奖

北京时间10月9日消息,瑞典皇家科学院决定将2019年诺贝尔化学奖授予约翰·古迪纳夫(John B。 Goodenough)、斯坦利·威廷汉(M。 Stanley Whittingham)和吉野彰,以表彰他们对锂离子电池的研究。这种可充电电池为手机和笔记本电脑等无线电子产品奠定了基础,还使一个无化石燃料的世界成为可能。从为电动汽车提供动力,到储存可再生能源,锂离子电池展现出了广泛的用途。
引言
电能为我们的生活提供了能量,无论何时何地,我们都需要电能。如今,即使附近没有电源插座,我们也可以十分方便、高效地获取电能。我们的移动方式越来越无拘无束,对电线的依赖也越来越少,可以在一个可能更健康的环境中享受高机动性。这一令人瞩目的发展是由高效的储能设备实现的。高容量电池使各种电动工具和车辆成为可能。原则上,我们都可以便捷地使用手机、相机、笔记本电脑、电动工具等,依靠高效的电池为它们提供动力。随着现代电池技术的发展,电动汽车也越来越受欢迎。我们正处在摆脱化石燃料汽车的时代。此外,有效的能源储存是对不稳定的能源(如风能和太阳能)的重要补充。有了电池,供需链可以随着时间的推移而平衡,即使在没有能源产出的情况下也是如此。
在很大程度上,锂离子电池使这些发展成为可能。这种电池彻底改变了能量存储技术,并促成了移动革命的实现。通过锂离子电池的高电势,高能量密度和高容量,这种电池类型为改善我们的生活做出了巨大贡献,并将在未来几年继续发挥作用。然而,总体而言,电池的发展非常艰巨且具有挑战性,尤其是锂电池。自1800年亚历山德罗·伏特提出他著名的“电池堆”以来,无数的科学家和工程师为电池的开发投入了巨大的努力。
从基本结构上,电池的工作原理是相对简单的。电池由两个电极组成,每个电极连接到一个电路,电解液可以容纳带电的物质。通常情况下,电极之间被一种隔离材料隔开,这种隔离材料可以防止电极之间的物理接触,从而避免电池短路。在放电模式下,当电池驱动电流时,负极(阳极)发生氧化过程,导致电子从电极流出并穿过电路。在正极(阴极)会发生一个互补的还原过程,从电路中获得电子。电池电压很大程度上取决于电极的电势差,整个过程是自发的。对于可充电电池,这一过程可以逆转,外加电流可作用于电极,产生互补的氧化还原反应。这个过程是非自发的,需要能量输入。
许多在学术界、工业界甚至是独立工作的科学家和工程师都为电池的发展做出了贡献,他们也深深理解开发高效电池是一项非常困难的任务。因此,电池发展相对缓慢,只有极少数有效的电池配置在设计成功后应用多年。例如,我们仍然依赖于19世纪中期发明的铅酸电池。尽管如此,通过一系列突破性的多学科科学发现,包括电化学、有机和无机化学、材料科学等,研究人员解决了诸多挑战,终于锂离子电池成为现实,从根本上改变了我们的世界。

背景
一种元素很少在戏剧中扮演核心角色,但2019年诺贝尔化学奖的故事中,有一个明确的主角:锂。这是一种在大爆炸的最初几分钟内产生的古老元素。1817年,当瑞典化学家Johan August Arfwedson和Jns Jacob Berzelius从斯德哥尔摩群岛乌托矿(Ut Mine)的矿物样本中提纯出这种物质时,人类才知道它的存在。
Berzelius将这种新元素命名为“lithos”,这个词在希腊语中意思是“石头”。尽管名字很厚重,但它却是最轻的固体元素。这也正是我们有时几乎不会注意到手机的原因。
更确切地说,瑞典化学家实际上并没有发现纯金属锂,而是发现了一种盐形式的锂离子。纯锂引发了许多火灾警报,尤其是在我们将要讲述的故事中;这是一种不稳定的元素,必须储存在石油中,这样才不会与空气发生反应。

锂是一种金属,其外电子层只有一个电子,因此有很强的动力把这个电子留给另一个原子。当这种情况发生时,就会形成一个更稳定的带正电荷锂离子。
锂的弱点是反应性,但这也是它的优点。20世纪70年代初, 斯坦利·威廷汉开发了第一块功能齐全的锂电池,他利用了锂释放其外层电子强大驱动力。1980年,古迪纳夫将电池的电势提高了一倍,为开发更强大、更实用的电池创造了合适的条件。1985年,吉野彰成功地从电池中去除了纯锂,而是完全基于锂离子,因为锂离子比纯锂更安全。
这使得锂电池成为了实际可行的电池。锂离子电池给人类带来了巨大的好处,使笔记本电脑、手机、电动汽车以及太阳能和风能的储存成为可能。
我们将回到50年前,回到锂离子电池最初的时代。
石油阴霾使电池研究重获新生

最初的可充电电池的电极中含有固体物质,当它们与电解液发生化学反应时就会分解。这一过程会损毁电池。斯坦利·威廷汉的锂电池的优点是,锂离子储存在阴极的二硫化钛空间中。当电池使用时,锂离子会从阳极的锂流向阴极的二硫化钛;而当电池充电时,锂离子又会回流。
20世纪中期,世界上使用汽油的汽车数量显著增加,汽车排放的废气使大城市里的有害雾霾更加严重。与此同时,人们日益认识到石油是一种有限资源。这一切都为汽车制造商和石油公司敲响了警钟。如果他们的企业要生存下去,就需要投资电动汽车和替代能源。
电动汽车和替代能源都需要强大的电池来储存大量的能量。实际上,当时市场上只有两种类型的可充电电池:早在1859年发明的铅酸电池(目前仍然用作燃油汽车的启动电池)和20世纪上半叶发明的镍镉电池。
石油公司投资新技术
面临石油枯竭的威胁,石油巨头埃克森(Exxon)决定将其业务多样化。在一项基础研究的重大投资中,埃克森公司招募了当时在能源领域最重要的一些研究人员,让他们可以自由地做几乎任何想做的事情,只要不涉及石油。
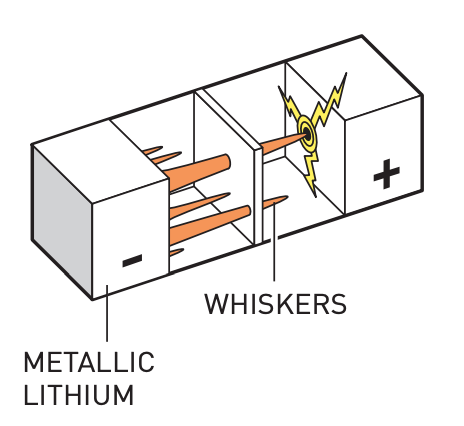
当以纯锂为阳极的电池充电时,会导致锂枝晶的形成。这些锂枝晶会使电池短路,引起火灾甚至爆炸。
斯坦利·威廷汉是1972年加入埃克森公司的科学家之一。他来自斯坦福大学,从事某些固体材料的研究。这些材料中具有原子大小的空间,可以让带电离子附着在上面。这种现象称为嵌入(intercalation)。当离子在材料内部被捕获时,材料的性质就会改变。在埃克森,斯坦利·威廷汉和同事开始研究超导材料,包括可以嵌入离子的二硫化钽。他们在二硫化钽中加入离子,并研究其电导率会受何影响。
威廷汉发现了一种能量密度极高的物质
就像科学上经常发生的情况一样,这个实验带来了一个意想不到的发现。原来钾离子会影响了二硫化钽的电导率。当斯坦利·威廷汉开始详细研究这种材料时,他观察到它有非常高的能量密度。也就是说,钾离子和二硫化钽之间的相互作用具有惊人的能量。当威廷汉测量这种材料的电压时,发现可达好几伏,这比当时的电池好多了。斯坦利·威廷汉很快意识到是时候改变方向了,他转向了能为未来的电动汽车储存能量的新技术。然而,钽是一种比较重的元素,而市场上不需要装载更重的电池。因此,他用钛代替了钽,钛的性质与钽相似,但重量轻得多。
作为负极的锂

古迪纳夫开始在锂电池的阴极中使用钴氧化物。这几乎使电池的电势翻了一番,使其更加强大。
于是,在锂离子电池的故事中,锂开始占据最重要的位置。作为斯坦利·威廷汉的新电池的负极,锂并不是一个随机的选择。在电池中,电子应该从负极(阳极)流向正极(阴极)。因此,负极应该使用一种很容易失去电子的材料,而在所有的元素中,锂是最愿意释放电子的元素。
这么做的结果就是,斯坦利·威廷汉开发出了一种可在室温下工作的可充电锂电池,它具有很大的电势,也具有巨大的潜力。他前往埃克森位于纽约的总部,就该项目进行了讨论。会议持续了大约15分钟,管理团队随后迅速做出决定:他们将利用斯坦利·威廷汉的发现开发一种具有商业可行性的电池。
电池爆炸和油价下跌
不幸的是,准备开始生产电池的小组遇到了一些困难。随着新的锂电池被反复充电,在锂电极上开始出现薄层的锂物质。当它们抵达另一个电极时,电池就会出现短路并引发爆炸。消防队不得不多次出动扑灭火灾,他们威胁要实验室支付用于扑灭这些锂电池大火所消耗的特殊化学物质的费用。为了让电池更加安全,在金属锂电极中加入了铝,两个电极之间的电解液也进行了更换。
斯坦利·威廷汉在1976年宣布了自己的发现,随后电池开始为一家瑞士钟表商进行小规模生产,并计划将其用于太阳能驱动的钟表当中。下一步的目标是扩充电池的容量,以便使其能够为汽车充电。但是在1980年代初,石油价格突然出现显著下降,埃克森公司需要削减成本。于是相关研究工作被停了下来,威廷汉所发明的技术被授权给了世界三个不同地区的三家不同的公司。但这并非意味着研究工作的终结。当埃克森公司放弃相关工作之后,约翰·古迪纳夫接手了。

吉野彰研制出了第一款可商用锂离子电池。他在阴极使用了古迪纳夫的锂-钴氧化物,并在阳极使用了一种名为石油焦的碳基材料,该材料中也可以插入锂离子。这款电池在发挥功能时,并不会发生破坏自身的化学反应。相反,锂离子可以在电极之间来回流动,使电池寿命大大延长
石油危机让古迪纳夫开始对电池技术感兴趣
还是一个孩子时,古迪纳夫在阅读方面存在明显障碍,这也是为何他会被数学吸引,并最终,在二战结束之后,开始研究物理学的原因之一。他在美国麻省理工学院林肯实验室工作多年。在此期间,他对随机存储器(RAM)的研究做出了贡献,时至今日RAM依旧是我们计算机中不可或缺的部件。
古迪纳夫和上世纪1970年代的许多人一样,都深深受到了石油危机的影响,于是他希望能够为能源的替代选择做出贡献。然而,林肯实验室是由美国空军资助的,并不允许从事这类研究。因此,当他被提供一个在英国牛津大学担任无机化学教授的机会时,他抓住了机会并最终一头扎进了重要的能源研究领域之中。
当锂离子与氧化钴结合时所产生的高电压
古迪纳夫知道威廷汉发明的革命性的新电池技术,但他对于物质内部结构的专业知识告诉他,如果电池的阴极用金属氧化物,而不是金属硫化物来制作,那么阴极的电势将可以更高一些。于是他的研究组的几位成员被交代了一项任务,寻找合适的金属氧化物,其应当可以在锂离子作用下可以产生比较高的电压,并且当这些离子被去除时也不会出现问题。
这一系统性搜寻的结果要比古迪纳夫原先设想的高得多。威廷汉的电池可以产生略多于2伏特的电压,但古迪纳夫发现,在阴极中使用钴酸锂材料的电池产生的电压将可以提升两倍,达到4伏特。在这其中的一项关键性发现是,古迪纳夫意识到,电池并不需要保持在充电状态下才能生产,而在此之前一直就是这样做的。相反,它们可以在被制造出来之后再充电。在1980年,他对外公布了这项全新的,高能量密度的阴极材料。尽管它分量很轻,却同样可以制造出性能强劲的电池。这是人类进入移动时代的关键一步。
日本公司迫切渴望轻质电池用于新型电子产品供电
然而,在西方,随着石油价格下探,对于寻找替代能源,以及开发不使用石油的电动车的投资热情开始出现下降。但是在日本,情况就完全不同。电子公司拼了命想要得到一种轻质,且可反复充电的电池,用于为他们的便携式摄像机,无线电话机和计算机供电。其中一个看到了这种巨大需求的人,便是日本旭化成株式会社的吉野彰。正如他自己所言的那样:“这就像嗅出趋势的大方向。你可以说,我这方面的嗅觉比较灵敏。”
吉野彰开发了第一个可商用锂离子电池
当吉野彰决定开发一种功能性可充电电池时,他选择了古迪纳夫的钴酸锂作为阴极,并尝试使用各种碳基材料作为阳极。此前研究人员已经证明,锂离子可以插入到石墨的分子层中,但是石墨会被电池的电解液分解。当吉野彰尝试使用石油焦(石油工业的副产品)时,他终于找到了灵感。他用电子给石油焦充电,发现锂离子被吸进了材料中。然后,当他打开电池时,电子和锂离子流向阴极的钴酸锂,而钴酸锂的电势要高得多。
吉野彰开发的电池具有工作稳定、重量轻、容量大的优点,能产生4伏的电压。锂离子电池最大的优点是离子能嵌入到电极上。其他大多数电池都是基于化学反应,而在化学反应中,电极会缓慢而稳定地改变。当锂离子电池充电或放电时,离子在电极之间流动,不与周围环境发生反应。这意味着电池的寿命更长,在充电数百次后性能才会下降。
另外一个巨大的优势在于,电池中不含有纯的锂。在1986年,当吉野彰在对电池的安全性进行测试时,他非常小心谨慎,甚至将检测工作放在一间专门用于爆炸物检验的房间内进行。他向电池投掷一大块铁,但是什么也没有发生。然而,当使用含有纯锂的电池进行重复试验时,电池发生了剧烈爆炸。通过安全性测试对于这款电池的未来前景极为关键。正如吉野彰所言的那样:这一刻,标志着锂电池正式诞生了。
锂离子电池——在无需化石燃料的社会中不可或缺
1991年,一家大型日本企业率先开始销售锂离子电池,在电子业引发了一场革命。手机体积得以缩小,电脑开始走向便携,MP3音乐播放器和平板电脑也逐渐问世。
在此之后,全世界的研究人员顺着元素周期表展开了依次搜索,试图研制出性能更优良的电池,但没有一种电池能在电池容量和电压上打败锂离子电池。不过,锂离子电池近年来也一直在革新和改进。例如,古迪纳夫将其中的氧化钴换成了磷酸铁,使电池变得更加环保。
就像几乎所有人类生产活动一样,锂离子电池的生产也对环境造成了一定影响,但也为环境带来了巨大的益处。有了锂离子电池,研究人员得以发明更清洁的能源技术和电动汽车,从而有力减少了温室气体和颗粒物的排放。
古迪纳夫、斯坦利·威廷汉和吉野彰通过他们的研究工作,为一个无线、无需化石燃料的新型社会创造了适当条件,极大地造福了全人类。(叶子,任天,晨风,未名)








